TEORI ATOM DALTON – Penelitian untuk menemukan berbagai pertanyaan “Apakah itu atom?” dilakukan terus-menerus seolah-olah tidak ada henti. Aristoteles dan Demokritus mengatakan bahwa atom merupakan benda terkecil dari suatu zat.
Mereka memberi nama dengan atomos. Setelah itu bermunculan tori-teori baru seperti Jhon Dalton hingga Niels Bohr.
Mari melihat kembali sejarah yang mengungkap fakta-fakta tentang teori atom.
1. Teori Atom Dalton
Pada Tahun 1808, seorang ilmuwan Inggris, John Dalton, mengemukakan teorinya tentang materi atom yang dipublikasikan dalam A New System of Chemical Philosophy.
Berdasarkan dari penelitian dan hasil perbandingannya, Jhon Dalton memberikan kesimpulan tentang atom beberapa point berikut :
1. Materi terdiri atas atom yang tidak dapat dibagi lagi.
2. Semua atom dari unsur kimia tertentu memiliki massa dan sifat yang sama.
3. Unsur kimia yang berbeda akan memiliki jenis atom yang berbeda.
4. Selama reaksi kimia, atom-atom hanya dapat bergabung atau dipecah menjadi atom-atom yang terpisah, tetapi atom tidak dapat dihancurkan dan tidak dapat diubah selama reaksi kimia tersebut.
5. Suatu senyawa terbentuk dari unsur-unsur dari gabungan atom tidak sejenis dengan perbandingan yang sederhana.
Teori Atom Dalton memiliki kelebihan dan kekurangan, Anda bisa membandingkannya pada perbandingan berikut ini.
Kelebihan Teori Atom Dalton
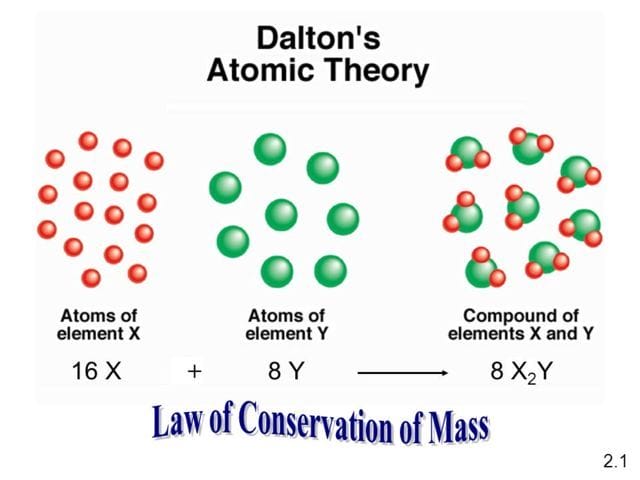
- Dapat menerangkan Hukum Kekekalan Masa (Hukum Lavoisier)
- Dapat menerangkan Hukum Perbandingan Tetap (Hukum Proust)
Kelemahan Teori Atom Dalton
- Tidak dapat menerangkan sifat listrik aotm
- Pada kenyataannya atom dapat dibagi lagi menjadi partikel yang lebih kecil yang disebut partikel subatomik.
2. Model Atom Thomson

Seorang ahli fisika berkebangsan Inggris, Joseph John Thomson, pada tahun 1897 menemukan sebuah elektron, suatu partikel lebih kecil dari atom yang bermuatan negatif.
Thomson mengungkapkan bahwa elektron merupakan partikel subatomik. Dari hasil penelitiannya inilah, Josep John Thomson memberikan hipoteis sebagai berikut “karena elektron bermuatan negatif, sedangkan atom bermuatan listrik netral, maka haruslah ada muatan listrik positif yang mengimbangi muatan elektron dalam atom”.
Maka Thomson mengusulkan suatu model atom yang terkenal dengan istilah model atom roti kismis.
- Atom berbentuk bola pejal bermuatan positif yang homogen (diibaratkan sebagai roti).
- Elektron bermuatan negatif tersebar di dalamnya (seperti kismis yang tersebar di dalam roti).
Dari dua uangkapan Thomson tersebut, ada beberapa kelebihan dan kelemahan dari teori yang ia uangkapkan. Kelebihan dan kekurangannya adalah sebagai berikut :
Kelebihan Teori Atom Thomson
Dapat menerangkan adanya partikel yang lebih kecil dari atom yang disebut partikel subatomik.
Dapat menerangkan sifat listrik atom.
Kelemahan Teori Atom Thomson
Tidak dapat menerangkan fenomena penghamburan partikel alfa oleh selaput tipis emas yang dikemukakan oleh Rutherford.